|
壹、 前言
惡性腫瘤一直為國民十大死亡原因之首,其中女性10 大癌症中,乳癌發生率占第一位,即每十萬人口中就會有56 位罹患乳癌,而乳癌死亡率更是高達第四名,1 可謂為國內女性同胞的頭號殺手。近來更發現台灣女性罹患乳癌年齡層有逐年下滑趨勢,其中罹癌的高峰期就足足比歐美國家早了10 歲,且每11 位乳癌患者中,就有一位小於35 歲,將近美國(3~4%)的3 倍,而造成此一結果之確切原因尚未定論,推測和遺傳、種族、生育率降低有莫大的關聯。
貳、 荷爾蒙治療沿革
停經前乳癌婦女使用荷爾蒙治療早已行之有年,最早在1896 年英國Dr. George Beatson就曾替三位婦女以卵巢摘除的方式來治療進展性的乳癌,是為荷爾蒙治療的先驅。然而近一世紀的發展中,因化學治療藥物發展崛起,讓荷爾蒙治療因此式微,而後在1974 年隨著荷爾蒙接受體的發現才又燃起生機。許多大規模的臨床試驗顯示,荷爾蒙接受體(Estrogen receptor,Progesterone receptor)顯示為陽性的患者,在接受輔助性荷爾蒙治療後,可以顯著的延長病患的無病存活期(disease free survival, DFS)和整體存活率(overall survival rate. OS)。而隨醫療技術日新月異,目前最常使用的荷爾蒙治療分為選擇性雌激素受體調節物(selective estrogen receptor modulator, SERM)和卵巢功能的抑制或根除(suppression/ablation)兩種方式。兩種方法對於抑制乳癌細胞的生長皆有不錯的治療效果,但對於停經前乳癌婦女治療所需考量的層面則相當複雜,這其中包含治療的時間,生育能力保存,提早進入更年期,病人無法接受的副作用等,都是目前所面臨到的問題。
參、 藥物治療
荷爾蒙治療在乳癌治療中目前仍定位在手術後/化療/放療後的輔助性治療。對於荷爾蒙接受體為陽性之停經前乳癌婦女應考慮使用荷爾蒙治療,而接受體為陰性之婦女則無法經由此種治療方式得到任何好處,反而會造成許多不必要的副作用。目前常見之治療方式如下:
一、選擇性雌激素受體調節物(selective estrogen receptor modulator, SERM)
藉由調節荷爾蒙接受體來抑制腫瘤細胞生長,最常見的使用藥物為tamoxifen。
大型臨床隨機分派研究和許多回溯性研究均證實給予tamoxifen 輔助治療停經前乳癌可以延長病人之無病存活率和整體存活率。New Zealand Guidelines Group(NZGG)建議停經前乳癌婦女在化療後應考慮給予tamoxifen 治療五年(NZGG grade A)。且對於那些tamoxifen使用五年後即將進入更年期狀態之婦女也建議可以持續使用芳香酶抑制劑aromatase
inhibitor),如anastrozole, letrozole 來抑制腫瘤細胞生長(NZGG grade A)。2
二. Ovarian suppression/ablation
(一) 排卵抑制(Ovarian suppression)
黃體素類似物(LHRH analogues or GnRH analogues)藉由干擾下視丘-腦下垂體-卵巢軸(hypothalamic–pituitary–ovarian axis)的方式來抑制雌激素(estradiol)的分泌(圖一),由於LHRH analogues 相較於內生性的LHRH 更能夠結合在LHRH 受體,導致持續性的刺激下視丘進而引發負向調節作用(downregulation),讓下游的gonadotropin 和estradiol 分泌減少,最後抑制腫瘤生長。此種治療方式好處在於讓卵巢呈現「睡眠」狀態,只要停止施打,絕大
多數女性均可回復原來月經周期,且相較於卵巢摘除副作用(骨質疏鬆、熱潮紅等更年期症狀)更低,對於期望生育之乳癌女性可以做為另一項選擇。3
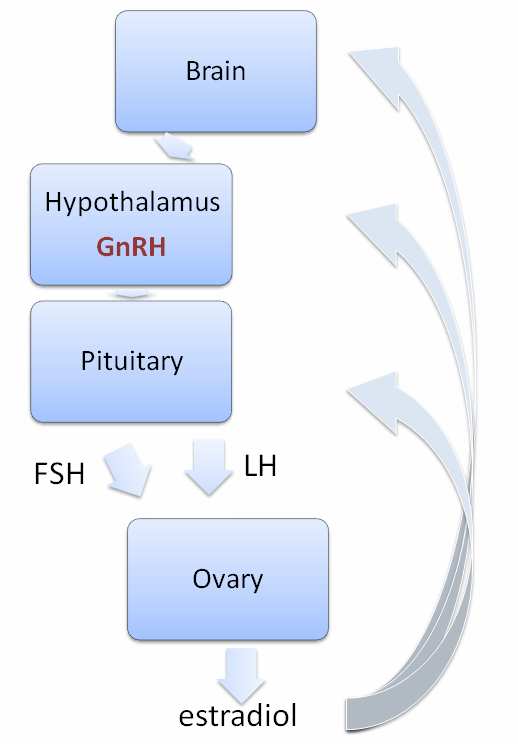
圖一、下視丘-腦下垂體-卵巢軸
許多研究(DynaMed 證據等級:level 2)指出無論是否有服用tamoxifen,停經前乳癌且荷爾蒙接受體為陽性之婦女在接受化學治療後,給予額外的LHRH analogues 可能降低死亡和乳癌復發之風險。也有許多研究(DynaMed 證據等級:level 2)指出LHRH analogues 對於小於50 歲尚未接受化學治療之乳癌婦女,可以降低復發之風險。2 針對小於40 歲以下之乳癌婦女,如果為復發高危險群,則可以在化療後考慮LHRH analogues(NZGG 證據等級B)。4
(二) 卵巢摘除(Ovarian ablation)
卵巢切除手術(Oophorectomy)一直被認為是種一勞永逸的方法,可以直接避免卵巢所分泌女性荷爾蒙去刺激乳癌細胞生長,術後女性將不再具有生殖能力,因此只要荷爾蒙接受體為陽性之乳癌婦女接受此一手術後,往後之處置可以比照停經後婦女治療方式給予tamoxifen 或aromatase inhibitor 治療。2008 年Journal of Oncology(JCO)一項大型臨床隨機研究分析指出,停經前乳癌婦女接受卵巢切除手術合併使用tamoxifen 治療,可以顯著地改善五年及十年之無病存活率和整體存活率。2
2003 年ZEBRA 研究發現停經前乳癌婦女若荷爾蒙接受體為陽性,卵巢摘除和化學治療效果相當,均可以改善無病存活率,而荷爾蒙接受體若為陰性則使用化學治療效果較好,其他研究似乎也指向此種結果。似乎卵巢摘除在治療方便性、花費上明顯優於其他治療方式。
但安大略省癌症醫護中心(Cancer Care Ontario, CCO)對於停經前乳癌婦女接受卵巢摘除卻持相當保留的態度,CCO 認為年輕女性若為早期侵犯性之乳癌,卵巢摘除不應作為常規性治療,除非病患拒絕接受其他全身性療法(化學治療或是放射線治療),卵巢摘除才可考慮做為替代性療法。5
眾多大型研究比較化學療法和Ovarian suppression/ablation 對於停經前乳癌婦女的無病存活期和整體存活率進行比較發現,傳統化學治療CMF(cyclophosphamide, methotrexate and fluorouracil)和Ovarian suppression/ablation 無論在DFS 或OS 表現結果相似(表一)。而2007年發表在Journal of Clinical Oncology中的臨床研究─TABLE發現荷爾蒙接受體為陽性之受試者,接受3 個月施打一次的leuprorelin 在OS 表現上甚至比CMF 還要來的優異。因此,若經
醫療專業評估後認為不適合接受化學治療之病患,荷爾蒙療法也可以作為另一項選擇。5
表一、藥物卵巢去勢VS.化學療法(Ovarian suppression versus chemotherapy)臨床研究5
| Study |
N |
Regimen |
Patient characteristics |
Results |
| ZEBRA |
1600 |
CMF × 6 (oral
or IV) vs
Goserelin ×
2 years |
Pre-/perimenopausal
Node(+)
HR+/− |
For HR+:
CMF = Goserelin
HR for DFS 1.05,
P = 0.597
HR for DDFS 1.03,
P = 0.749
For HR−:
CMF> Goserelin
HR for DFS 1.83,
P = 0.0001
HR for DDFS 1.65,
P = 0.0028 |
| TABLE |
599 |
CMF × 6 (IV)
vs
Leuprorelin ×
2 years |
Pre- or perimenopausal
ER+
Node(+) |
CMF= Leuprorelin
HR for RFS 1.19,
P = 0.15
HR for survival 1.50,
P = 0.005
(OS analysis was exploratory) |
DFS = Disease-free survival; DDFS = Distant disease-free survival; RFS = Relapse-free survival;
Survival = Overall survival, EFS = Event-free survival, HR = Hazard ratio,
RR = relative risk.
a. Dose of goserelin is 3.6 mg depot subcutaneously every 28 days.
b. Defined as age <50 years.
c. Leuprorelin acetate depot 11.25 mg subcutaneously every 3 months.
d. Goserelin 3.6mg subcutaneously every 28 days. |
参、治療計畫
停經前乳癌婦女使用荷爾蒙治療時機,約在手術/化療/放療後作為輔助性治療,如使用卵巢抑制(ovarian suppression)的方法,目前最常為LHRH analogues 與tamoxifen 合併使用三年(tamoxifen 使用五年)。100 年2 月健保也通過goserelin 給付用於停經前(或更年期前)之早期乳癌,但須符合下列六項規定:
1. 與tamoxifen 合併使用,作為手術後取代化學治療之輔助療法。
2. 荷爾蒙接受體為強陽性:ER/PR 為2+或3+。
3. Her-2 Fish 檢測為陰性或IHC 為1+。
4. 淋巴結轉移數目須≦3 個。
5. 使用期限:goserelin 使用3 年,tamoxifen 使用5 年。
6. 須事前審查,並於申請時說明無法接受化學治療之原因。
而若使用tamoxifen 達五年且即將進入更年期,也可以轉換芳香酶抑制劑(aromatase
inhibitor)做進一步的治療。4
肆、 副作用
停經前婦女接受荷爾蒙治療最常見之副作用包括熱潮紅、骨質密度流失、子宮內膜增生、陰道出血、增加靜脈栓塞危險等副作用。4
一項大型臨床隨機研究(ABCSG-12 trial)發現,荷爾蒙治療期間(使用tamoxifen 或aromatase inhibitor)給予zoledronic acid 可以顯著改善停經前早期乳癌婦女的無病存活期和在荷爾蒙期間所造成的子宮內膜增生。歐洲內科腫瘤醫學(European Society for Medical Oncology, ESMO)也建議使用zoledronic acid 來預防骨質疏鬆和降低乳癌復發的機率。6
伍、 保存生育
越來越多的婦女在生育之前或懷孕期間,發現自己得到乳癌,這些患者也因此會顧慮接受化學治療是否會影響胎兒,或是擔心接受化學治療和荷爾蒙治療影響未來生育機會。
有些化學治療藥物如烷基化合物(alkylating agents),尤其是cyclophosphamide 容易影響到卵巢功能。這些化療藥物主要藉由影響卵泡成熟過程,或是破壞卵泡造成暫時性或是永久性的停經。研究顯示合併化療CMF(cyclophosphamide+methotrexate+5-flurouracil),對於40 歲以下之年輕乳癌女性有20~70%機率造成停經作用。而以蒽環類(anthracycline)為基礎的合併化學治療所造成的停經發生率反而較少,推測以此為基礎的合併化學治療可以減低cyclophosphamide 的使用劑量,進而減低藥物對卵巢功能所造成的損傷。但對於紫杉醇類化療藥物所造成停經目前尚未有明確定論。
乳癌病患使用tamoxifen 期間是否可以正常懷孕?動物研究顯示出使用tamoxifen 會造成胎兒泌尿生殖系統異常,而人類也有極少數案例發生胎兒顱面或生殖泌尿道異常狀況。因此,在使用tamoxifen 治療的五年期間,仍建議治療完成後再考慮懷孕,唯五年期間對女性而言,實是一大挑戰。
許多小型研究發現在化療期間給予LHRH analogues 有保護卵巢的功能。2008 年一項小型隨機臨床研究發現停經前婦女化學治療前給予LHRH analogues 有助於回復排卵和月經周期,但這項結果目前仍需更多研究去證實。
女性的生育能力,在三十七歲以後會快速下降。為了怕耽誤生育的黃金年齡,有幾種保留生殖能力的方法可以考慮:胚胎冷凍保存、冷凍保存卵子(表二)。冷凍保存的胚胎或卵子只能用來幫助懷孕,卻無法恢復病患的卵巢功能,病患還是要面臨更年期的一些症狀。針對以上這些問題,可以由卵巢組織冷凍保存技術來加以解決。這個技術是在病患接受化療前利用手術取出一部分卵巢組織加以冷凍保存,等治療結束後再將卵巢組織植入體內。這樣可以幫助病患恢復卵巢功能及週期性的排卵,而且有機會可以自行懷孕。7
表二、現行保存生育技術之優缺點7
| 處置 |
好處 |
壞處 |
| 體外受精與冷凍胚胎保存 |
1. 懷孕機率相對較高 |
1. 須男性伴侶且須從雙方合法取得胚胎
2. 可能會讓體內女性激素濃度上升進而刺激癌細胞生長
3. 若基因發生突變,則後代罹癌危險機率上升 |
| 刺激排卵與卵細胞冷凍保存 |
1. 不須男性伴侶 |
1. 極少成功案例
2. 可能會讓體內女性激素濃度上升進而刺激癌細胞生長
3. 若基因發生突變,則後代罹癌危險機率上升
4. 可能會延誤化學治療 |
| 卵巢組織冷凍保存技術和與異種移植 |
1. 不須男性伴侶
2. 不須刺激卵子生成和提高雌激素濃度
3. 較不會延誤化學治療 |
1. 極少成功案例
2. 移植的卵巢組織可能會受到癌細胞的微轉移而造成影響
3. 若基因發生突變,則後代罹癌危險機率上升
4. 過程需動手術 |
| 利用黃體類似物來抑制排卵(保護卵巢細胞不受破壞) |
利用黃體類似物來抑制排卵(保護卵巢細胞不受破壞) |
1. 仍需更多臨床實驗去證實其有效性
2. 確切產生的副作用目前仍未知 |
至目前為止,尚未有任何一個治療方法可以保證乳癌婦女可以完全保存生育能力;和罹患其他癌症且考慮生育的患者相比,尤其是荷爾蒙接受體為陽性的女性乳癌患者,在接受治療期間往往要考慮保存生育能力,同時防止乳癌復發,相較之下更是複雜許多。
陸、結論
儘管荷爾蒙治療在停經前乳癌婦女已有一百多年的歷史,但最佳的治療方式目前仍無法釐清。在現今治療方面上,無論是使用tamoxifen 或是其他ovarian suppression 以及化學治療皆有一定的潛力。雖然過去許多研究對於停經前乳癌婦女均著重在化學治療,但近年來荷爾蒙治療逐漸崛起並深具發展價值。而如何善用各種治療方式並考量病患未來生育能力,是往後研究的發展方向。
柒、參考文獻
1. 行政院衛生署國民健康局健康統計資訊-97 年癌症登記報告。Available at http://www.bhp.doh.gov.tw/bhpnet/portal/Statistics.aspx. Accessed Sep, 2011.
2. DynaMed 實證醫學資料庫。Accessed Sep, 2011.
3. Goldman L, Ausiello D. Cecil Medicine - 23rd Edition, Saunders, 2007: 1814.
4. New Zealand Guidelines Group (NZGG). Management of Early Breast Cancer 2009
5. Shannon P, Adam B, Nancy D. Adjuvant endocrine therapy for premenopausal women with
breast cancer. The Breast 18 2009;S3: 122–130.
6. Michael G, Brigitte M, Herbert S, et al. Adjuvant endocrine therapy plus zoledronic acid in premenopausal women with early-stage breast cancer: 62-month follow-up from the ABCSG-12 randomised trial. Lancet Oncol 2011; 12: 631–41.
7. M. Hickey, M. Peate, C.M. Saunders, Breast cancer in young women and its impact on reproductive function. Human Reproduction Update 2009;15: 323–339.
|