|
一、前言
隨著人口的老年化,以及生活壓力的劇增,不時會有民眾誤服過量的藥品,因此產生不良反應而送至本院急診。面對不同的狀況,藥師常會接到相關的藥物諮詢,尋求處置建議,此時,藥師應迅速提供正確及明確的藥物處置建議,以幫助其他醫療人員正確處置病人的藥物過量。接下來,本文將就本院常見藥物過量的處置來討論。
二、各論
Acetaminophen
症狀
24小時內多為胃腸道方面的不良反應,如噁心,想吐,意識大多仍保持清醒,而肝功能指數(AST / ALT)多在48小時後,才會明顯的上升。
處理原則
1.先確認病患服用的時間,抽血分析Acetaminophen 血中濃度。
2.服藥一小時內,可以先使用活性碳(activated charcoal)洗胃,減少剩餘藥物的吸收。
3.抽血測量 Acetaminophen、AST、ALT、bilirubin、prothrombin time、Cr、BUN、 blood sugar 及電解質等數據。監測病人的肝功能、腎功能、 電解質及體液的平衡。
4.給予N-acetylcysteine,8小時內給予效果最好,24小時內給予仍然有效。
(1) 口服
•治療負載劑量(Loading dose):140 mg/kg。
•之後每四小時的維持劑量(Maintain dose):70mg /kg 共17個劑量。 [註] 參考國外口服溶液的濃度,建議調配5%濃度,以避免發生嘔吐。
(2)注射
•Initial dose: 150 mg / kg in D5W (1:1) 靜脈滴注15 分鐘。
•接著50 mg / kg in D5W 500 ml靜脈滴注4 小時。
•最後100 mg /kg in 1000 ml D5W 靜脈滴注16小時 (共20小時,總量300 mg /kg)。
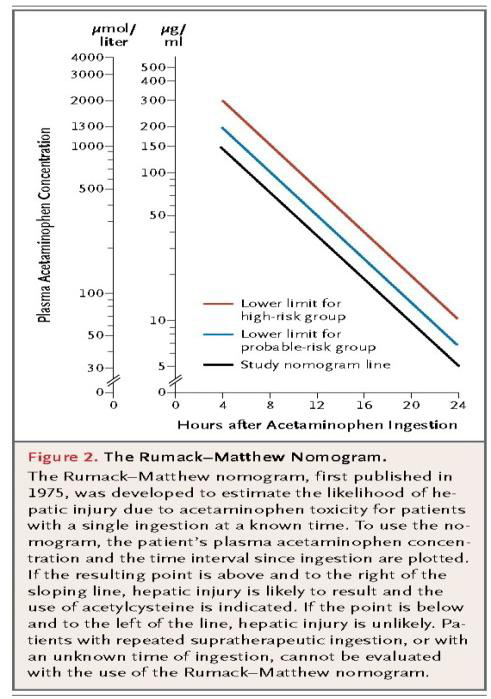
5.抽血測量 Acetaminophen並以Matthew-Rumack曲線 [圖一]修正。若病患的 Acetaminophen 血中濃度在毒性範圍,應每天測量 AST、ALT、bilirubin、 prothrombin time、Cre、BUN、blood sugar 及電解質等數據;若病人的Acetaminophen 血中濃度不在毒性範圍,則可停止使用Acetylcysteine 的療程。
[註] 血中濃度<150mcg/ml 可不必治療,若血中濃度介於150-200mcg/ml 間,建議給予治療,濃度若>200mcg/ml,毒性症狀會出現。
[圖一] Matthew-Rumack
Digoxin
症狀
腸胃道症狀:噁心嘔吐,厭食。視力模糊,甚至會看到黃綠閃光,或是出現紅綠色盲。中樞神經:虛弱,嗜睡,頭暈。ECG:Ventricular premature contraction(VPC),二度或三度的AV
block,junctional rhythm, atrial tachycardia (AT),ventricular tachycardia (VT)。
處理原則
1.先確認病患服用的時間,若剛服用可催吐,並以活性炭洗胃(此處置可能會引起交感神經刺激,如果病人已有心房心室阻斷症狀時,應避免。)
2.抽血分析 digoxin 血中濃度SDC(藥 物分布緩慢,半衰期長,約12-24小 時間一次),監測腎功能Cre、BUN 及電解質(尤其Ca,K,Mg,當低 血鉀、低血鎂及高血鈣時,會使過量 毒性症狀加劇)等數據。監測病人的 心臟功能、腎功能、電解質及體液的 平衡。
3.確認會加劇毒性藥物的使用必要性,如抗心律不整(amiodarone) 、降血壓藥物(verapamil, diltiazem, beta-blocker)、抗生素( amphotericin B )、利尿劑,以避免症狀加劇。
4.必要時,可考慮血液透析,但由於digoxin分布體積大,透析效果有限,無法有效全數清除。
5.依心臟症狀表現,給予適當藥物與 處置,校正電解質,以緩解竇性徐 脈為例,給予atropine 0.5-1 mg (小孩 0.02 mg/kg) 靜脈或經氣管吸入,需 要時可每五分鐘一次。
6.如果無法緩解或是嚴重中毒濃度(> 15ng/ml)給予digoxin immune Fab (Digibind),約36-40mg 的 digibind 約可以抓取 0.5-0.6mg的digoxin。
[劑量]
•根據血中濃度:digibind瓶數 (40 mg/vial) = 監測到血中濃度SDC (ng/ml) x 體重(kg)/100。
•根據吃的量:以0.25 mg/tab而言,吃5顆用2瓶,吃10顆用4瓶,吃25顆用10瓶,以此類推。
Organophosphate insecticides
症狀
會在接觸到毒物後數秒鐘到12小時內出現,中毒症狀的表現,主要涵蓋muscarinic/nicotinic/ CNS等三個系統:
(1)蕈毒樣作用(Muscarinic effect): 流汗、流淚、口水增加、視力模糊、縮瞳、胸悶、呼吸困難、肺部分泌物增加、心跳變慢、血壓降低、噁心、腹痛、腹瀉及大小便失禁。
(2) 菸鹼樣中毒作用(Nicotinic effect): 肌肉無力、局部肌肉抽動、抽痙、痙攣、麻痺及交感神經亢奮作用。
(3) 中樞神經作用: 頭暈、頭痛、焦慮不安、嗜睡、神 智不清、昏迷、休克及呼吸衰竭等。
處理原則
1.有機磷會經由皮膚吸收,故需迅速以肥皂洗淨病患全身;為防中毒,醫護人員須戴口罩及手套。
2.確保呼吸道暢通,必要時,抽吸口腔及氣管內的分泌物。若病人意識不清或呼吸衰竭則須插管,並監測呼吸功能(包含動脈血分析)及生命徵象。
3.給予抗膽鹼(anticholinergic)藥物。
•Atropine可以拮抗ACh而改善有機磷造成的 muscarinic effects,由於結構為三級胺,亦可以通過血腦障壁BBB對中樞產生作用,因此能減少氣管內的分泌物、減少口水、流汗等情形,改善噁心、嘔吐、脈搏緩慢等作用。
[劑量] 兩種給法
(1) 1-2 mg 靜脈注射,視情況每15分鐘 至 2小時追加直到atropinization。 (小孩 0.015∼0.05 mg/kg)
(2)1.2-1.5 mg/hr 靜脈持續輸注。
[註] Atropine可通過血腦障蔽(BBB),過量時可能會有中樞神經的副作用,其表現包括發燒、意識改變、心跳過快、皮膚乾熱、吸氣會喘、高血壓、口乾、瞳孔放大或沒有反應等不良反應,所以使用atropine治療時請務必注意atropine的副作用反應。
•Glycopyrrolate結構為四級胺,因此不會穿透至中樞系統,主要改善週邊的muscarinic effects,不會產生中樞毒性,在雙盲試驗中,其效果與atropine沒有顯著上差異,故可用來作為atropine發生不良反應時的替代治療選擇,亦有文獻將其與atropine併用(atropine : glycopyrrolate = 2:1),但仍須更多的大型研究來證實。
[劑量] 兩種給法,口服吸收差,不考慮使用。
(1)1mg IV bolus每10-15分鐘,直到muscarinic effects症狀緩解。
(2)1mg IM每30-40分鐘,直到muscarinic effects症狀緩解。
•Pralidoxime (2-PAM) 主要針對nicotinic作用,藉由移除化合物中的有機磷根,翻轉cholinesterase被抑制的情形而重新活化cholinesterase的作用,改善有機磷造成的nicotinic effect,如呼吸抑制或肌肉無力等症狀。
[劑量]
(1) 急性投與: 30 mg/kg (約1-2 g稀釋於 100-150 ml生理食鹽水) IV滴注30分 鐘以上,視情況,之後每4-6小時給 予一次。
(2)持續輸注: 8-10 mg/kg/hr,10 amps (5 g) + NS 400 ml (總體積為500 ml) 最終濃度為10 mg/ml;以60公斤的病人為例,約40-60 ml/hr流速持續輸注 (小孩劑量 5-10 mg/kg/hr) 。 [註] A.儘量在投與2-PAM之前使用atropine,。 B. 除非病患非常危急,否則避免快速IV bolus給予2-PAM,給予速率過快可能會產生神經肌肉阻斷作用或是心臟抑制。 C. 最好在24-48小時內投與,尤其是中毒的6小時內投與最有效。 D. 其代謝產物可能造成噁心、頭暈、意識不清等副作用症狀,常難與有機磷中毒症狀區分。
4.應監測心跳 (應維持在80-120/min, 需要持續監控ECG來評估心臟狀 態)、意識(需回復到清醒)呼吸 音,以及acetylcholinesterase。另外,呼吸衰竭可能在有機磷中毒好幾天過後才出現,且症狀會持續數天至數週 縱使中毒症狀已改善,仍需小心監控病患肺部氣體交換狀況,尤其當病患服用大劑量有機磷造成中毒時,除此之外,應注意胰臟炎、癲癇、次發性的感染,如肺炎、敗血症等併發症的發生。
5.注意其他可能會加重有機磷作用的藥物,例如 physostigmine 或 succinylcholine 及 antihistamine類等。
三、 Reference
1.Bardin PG, van Eeden SF. Organophosphate poisoning: grading the severityand comparing treatment between atropine and glycopyrrolate. Cfit Care Med 1990; 18: 956-60.
2.ThompsonDF, ThompsonGD, GreenwoodR.B,Trammel HL. Therapeutic dosing of pralidoxime chloride. Drug Intelligence and Clinical Pharmacy 1987; 21: 590-3.
3.TraceyJA, GaUagherH. Use of glycopyrrolate and atropine in acute organophosphorus poisoning. Hum Exp Toxicol 1990; 9: 99-100.
4.Choi PT, Quinonez LG, Cook DJ, Baxter F, Whitehead L The use of glycopyrrolate in a case of intermediate syndrome following acute organophosphate poisoning Can J Anaesth. 1998 Apr;45(4):337-40.
5.Robenshtok E, Luria S, Tashma Z, Hourvitz A Adverse reaction to atropine and the treatment of organophosphate intoxication Isr Med Assoc J. 2002 Jul;4(7):535-9.
6. Kennon J. Heard, M.D. Acetylcysteine for Acetaminophen Poisoning N Engl J Med. 2008 July 17; 359(3): 285–292.
7.Ip D, Syed H, Cohen M.Digoxin specific antibody fragments (Digibind) in digoxin toxicityBMJ. 2009 Sep 3;339:b2884. doi: 10.1136/bmj.b2884.
8.Tripathi M, Pandey R, Ambesh SP, Pandey M. A mixture of organophosphate and pyrethroid intoxication requiring intensive care unit admission: a diagnostic dilemma and therapeutic approach Anesth Analg. 2006 Aug;103(2):410-2, table of contents
9.Weinbroum AA. Pathophysiological and clinical aspects of combat anticholinesterase poisoning Br Med Bull. 2005 Apr 21;72:119-33. Print 2004
10.Ehle M, Patel C, Giugliano RP. Digoxin: clinical highlights: a review of digoxin and its use in contemporary medicineCrit Pathw Cardiol. 2011 Jun;10(2):93-8. doi: 10.1097/HPC.0b013e318221e7dd.
11.Keays R, Harrison PM, Wendon JA, Forbes A, Gove C, Alexander GJ, Williams R ntravenous acetylcysteine in paracetamol induced fulminant hepatic failure: a prospective controlled trial BMJ. 1991 Oct 26;303(6809):1026-9.
12.Kerr F, Dawson A, Whyte IM, Buckley N, Murray L, Graudins A, Chan B, Trudinger B. The Australasian Clinical Toxicology Investigators Collaboration
|